GIẢI PHÁP XỬ LÝ AMONI VÀ PHOTPHO
Trong số các chỉ tiêu ô nhiễm, chỉ tiêu ô nhiễm Amoni và Photpho cũng là 2 yếu tố quan trọng cần xử lý triệt để. Các giới hạn cho phép xả thải đối với Amonia ngày càng trở nên nghiêm ngặt hơn, khiến việc xử lý Amoni và Photpho trở thành một trong những quy trình quan trọng nhất và khó khăn nhất đối với các trạm xử lý nước thải.

Tác động của nước thải chứa Amoni và Photpho đến môi trường và con người
Amoni là một trạng thái hóa trị của nitơ, tồn tại ở hai dạng là ion NH4+ và dạng khí NH3 chiếm đến 90 – 97% tổng nito. Ion NH4+ ít độc, NH3 là chất khí có mùi khai, không màu, tan nhiều trong nước, gây độc chết sinh vật trong nước. NH3 chiếm ưu thế khi ở trong môi trường pH cao (pH ≈ 11), trong môi trường pH thấp thì NH4+ chiếm ưu thế hơn (pH ≈ 7).
Khi tồn tại ở nồng độ cao, amoni rất dễ chuyển hóa để tạo thành các gốc nitrit NO2- và nitrate NO3-. Qua quá trình ăn uống, các chất này sẽ hấp thu vào trong cơ thể và gây ra một số bệnh n
guy hiểm và chuyển hóa thành các chất gây ung thư.
Photpho thường tồn tại dưới dạng photphat hòa tan: orthophotphat, meta hoặc poliphotphat và photphat hữu cơ.
Amoni cùng với Photpho chưa được xử lý nếu xả thải ra ao, hồ, kênh rạch sẽ trở thành nguồn dinh dưỡng cho các thực vật phù du, rêu, tảo phát triển mạnh mẽ, gây ra hiện tượng phú dưỡng hóa. Phú dưỡng hóa làm giảm nồng độ oxy hòa tan trong nước, một số loài tảo gây độc ảnh hưởng trực tiếp đến các động vật thủy sinh, thậm chí có thể gây chết và ô nhiễm nước ngược trở lại.
Trong quy chuẩn QCVN 01:2009/BYT ngày 17 tháng 6 năm 2009 đối với nước ăn uống quy định nồng độ amoni có trong nước
không được vượt quá 3 mg/L.
Trong QCVN 40: 2011/BTNMT đối với nước thải công nghiệp quy định nồng độ amoni có trong nước thải sau xử lý không vượt quá 5 mg/L. Photpho không vượt quá 4 mg/l
Phương Pháp Xử Lý Amoni
Cơ Sở Xử Lý Amoni
Để xử lý amoni trong nước thải có thể sử dụng nhiều phương pháp như phương pháp hóa lý, hóa học hay phương pháp sinh học. Nguyên lý chung của các phương pháp này là chuyển amoni thành các chất khác hoặc tách chúng ra khỏi môi trường nước.
Việc lựa chọn phương pháp xử lý phù hợp dựa vào nồng độ amoni có trong nước cũng như về chi phí đầu tư. Nếu nồng độ amoni không cao (< 100 mg/l) như trong nước thải sinh hoạt thì sử dụng phương pháp vi sinh là thích hợp nhất, nồng độ ammoni từ 100 – 5.000 mg/l cũng sử dụng phương pháp vi sinh hoặc có thể sử dụng phương pháp sục khí bay hơi, nồng độ ammonium lớn hơn 5.000 mg/l nên sử dụng phương pháp hóa lý sẽ phù hợp cả về mặt kỹ thuật lẫn kinh tế.
1- Phương Pháp Hóa Lý
- Tripping điều khiển pH: Chính là nâng độ pH lên đến 11 để chuyển hóa NH thành NH. Tuy nhiên, hiệu quả khó đạt đến 80%.
- Tripping điều khiển nhiệt độ: Cấp nhiệt cho nước thải, hiệu quả xử lý đạt đến 98%. Tuy nhiên, phương pháp này lại tiêu tốn mức chi phí đầu tư lớn.
- Trao đổi ion: Các ion amoni hoán đổi với các cation trong zeolit. Zeolite là một dạng tinh thể của một khoáng aluminosilicate cấu trúc khung anion xốp. Quá trình này thường được cạn kiệt và zeolit thường phải cần tái sinh thường xuyên.
Zeolite NH4+ quá trình trao đổi có thể được thể hiện bằng công thức: X + Z- + NH4 + → NH4 + Z- + X+
- Trong đó: Z đại diện cho aluminosilicate anion, X đại diện cho trao đổi ion.
- Quá trình này thường được cạn kiệt và zeolit thường phải cần tái sinh thường xuyên.
2- Phương Pháp Hoá Học
- Phương pháp Clo hóa
Phương pháp clo hóa được coi là phương pháp khử amoni hiệu quả nhất khi clo gần như là hóa chất duy nhất có thể oxy hóa amoni ngay ở nhiệt độ phòng để tạo khí N2 dễ bay hơi. Tốc độ phản ứng của clo với amoni cũng nhanh hơn so với các chất hữu cơ. Lượng clo cho vào nước thải so với amoni tương ứng với tỷ lệ 8:1. Phương pháp này hiệu quả với chi phí rẻ. Tuy nhiên nó lại có nhược điểm là khi lượng amoni hết, clo dư sẽ phản ứng với các chất hữu cơ có trong nước để tạo ra các hợp chất có mùi khó chịu, trong đó khoảng 15% các chất thuộc nhóm THM – trihalomethane và HAA – axit axetic halogen hoá đều có khả năng gây ung thư. Do đó trong quá trình sử dụng người vận hành cần có kỹ thuật tốt và hết sức cẩn thận.
- Phương pháp Ozone hóa
Sử dụng Ozone là chất oxi hóa mạnh để oxi hóa Amoni thành N2, phương pháp này an toàn và không tạo ra sản phẩm phụ độc hại như Clo. Đồng thời Ozone cũng dùng để khử trùng, khử màu, mùi và các chất hữu cơ khó xử lý khác. Tuy nhiên chi phí đầu tư cao, ít ứng dụng cho xử lý nước thải.
3- Phương pháp điện hóa
Để xử lý amoni trong nước thải có một số nghiên cứu áp dụng pha nước thải với 20% nước biển và đưa vào bể điện phân với anot than chì và catot inox. Dưới tác dụng của dòng điện sẽ tạo thành magie hidroxit, chất này phản ứng với amoni và photpho trong nước thải tạo thành thành phần không tan là magie amoni photphat. Ngoài ra quá trình điện phân còn hình thành Cl2 có thể oxy amoni, các chất hữu cơ và diệt khuẩn cho nước thải.
Hiệu suất xử lý amoni của phương pháp này đạt 80 – 85%, hiệu điện thế sử dụng khoảng 7V, tiêu tốn điện năng ở mức 200A/h cho 1 m3 nước thải.
Chất kết tủa tạo thành có thể sử dụng làm phân bón.
Xem thêm: Phương pháp điện hóa
4- Phương Pháp sinh học
- Quá trình nitrat hóa và khử nitrat

*Quá trình nitrat hóa
Quá trình oxy hóa amoni thành nitrit (do vi khuẩn nitrosomonas) và tiếp tục thành nitrat (vi khuẩn nitrobacter) phụ thuộc trực tiếp vào nồng độ oxy hòa tan pH, nhiệt độ,… Quá trình này xảy ra ở bể hiếu khí.
Bước 1. Vi khuẩn nitrosomonas sẽ chuyển hóa amoni thành nitrit
NH4+ + 1,5O2 → NO2– + 2H+ + H2O
Bước 2. Vi khuẩn nitrobacter sẽ chuyển hóa nitrit (NO2– ) thành nitrat (NO3– )
NO2– + 0,5O2 → NO3–

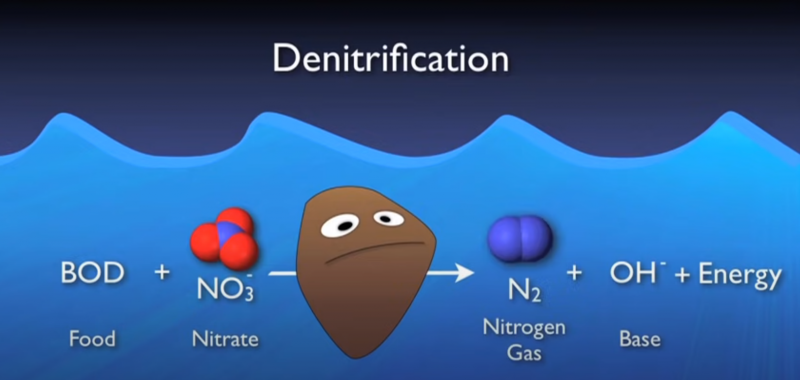
*Quá trình khử nitrat
Là quá trình vi sinh chuyển hoá các dạng NO3–, NO2–, NO, N2O về dạng N2 hay quá trình khử nitơ từ dạng hoá trị dương về dạng hoá trị kh
ông. Trong môi trường thiếu oxy, xảy ra ở bể Anoxic, các loại vi khuẩn này sẽ khử Nitrat (NO3-) và nitrit (NO2-) theo chuỗi chuyển hóa:
NO- → NO2- → NO → N2O → N2↑
Khí nitơ phân tử N2 tạo thành sẽ thoát khỏi nước và ra ngoài. Như vậy là nitơ đã được xử lý. Vi sinh vật thực hiện quá trình khử Nitrat có tên chung là Denitrifier bao gồm ít nhất là 14 loại vi sinh vật có thể khử nitrat như Bacillus, Pseudomonas, Paracoccus, Spirillum, Thiobacillus,.. phần lớn chúng thuộc loại tuỳ nghi, tức là sử dụng nguồn cacbon hữu cơ để tổng hợp tế nào một số ít thuộc loại tự dưỡng.
Hình mô tả vi khuẩn khử nitrat
Yếu tố quan trọng liên quan đến quá trình khử nitrat là cơ chất (chất hữu cơ, CH3OH), và kiểm soát nồng độ oxy trong nước để hiệu quả khử nitrat được tối ưu.
Trong thực tế, các kỹ sư công nghệ thường áp dụng các công trình tổng hợp để kết hợp xử lý BOD/Amoni trong cùng cụm bể.
- Công nghệ A-O ứng dụng quá trình nitrat hóa/khử nitrat xử lý Amoni
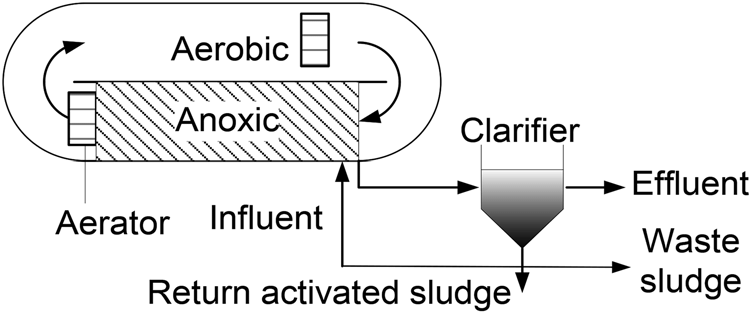
Công nghệ AO là viết tắt của Anoxic (Thiếu khí) – Oxic (Hiếu khí) là sử dụng cụm bể Anoxic sử dụng các vi khuẩn thiếu khí để khử nitra thành N2 và theo sau là bể Oxic chứa các vi khuẩn hiếu khí chuyển hóa amoni thành nitrit, nitrat.

Hình mô tả AO
Nitrat hóa xảy ra trước, khử nitrat xảy ra sau, vậy tại sao các bể lại thiết kế dạng A-O (thiếu khí trước – hiếu khí sau)
Nếu quá trình xử lý hiếu khí trước, BOD có thể mất hết mà N mới chỉ ở dạng NO3-, chưa tách thành dạng N2 tự do. Khi đó nước thải sau xử lý sẽ đạt chỉ tiêu BOD và Amoni, nhưng không đạt chỉ tiêu Nitrat.
Do đó trong thiết kế thông thường, để giảm thể tích các bể chứa người ta thiết kế bể Anoxic trước bể Oxic, việc chuyển hóa từ NO3- thành N2 diễn ra trong bể Anoxic nhờ dòng bơm tuần hoàn.
- Công nghệ mương oxi hóa
Mương oxy hóa là một trong những phương pháp xử lý nước thải theo phương pháp sinh học. Và là dạng cải tiến của bể aerotank với việc khuấy trộn và kéo dài chế độ làm việc làm thoáng. Nhằm xử lý triệt để Ni tơ Amoni bên cạnh việc xử lý các chất hữu cơ.
Hình mô tả mương oxi hóa
Mương oxy hóa có hiệu quả xử lý BOD5 nitơ cao, dễ quản lý thời gian, ít bị ảnh hưởng bởi sự dao động của lưu lượng nước thải đầu vào. Nên các khu vực xử lý nước thải có diện tích xây dựng lớn thường được ưu tiên xây dựng hệ thống mương oxy hóa để tối ưu hiệu quả xử lý nước thải.
Phương Pháp Xử Lý PhotPho
CƠ SỞ XỬ LÝ PHOTPHO
Hầu như tất cả các hợp chất của photpho không tồn tại ở dạng bay hơi trong điều kiện thông thường, vì vậy để tách photpho ra khỏi nước cần phải chuyển hóa chúng về dạng không tan trước khi áp dụng các kỹ thuật tách chất lắng như: lọc, lắng hoặc tách trực tiếp qua màng thích hợp.
Hợp chất photpho trong môi trường nước thải tồn tại trong các dạng: photpho hữu cơ, photphat đơn (H2PO4-, HPO42-, PO43-) tan trong nước, polyphotphat hay còn gọi là photphat trùng ngưng, muối photphat và photpho trong tế bào sinh khối.
Loại bỏ photpho bằng phương pháp hóa học
Để loại bỏ photpho, người ta có thể dùng phèn, muối sắt hoặc vôi để kết tủa hóa học. Đây được xem là phương pháp lâu đời nhất để giảm photpho hòa tan trong nước thải. Sử dụng phèn hoặc muối sắt được dùng nhiều hơn vì chúng hoạt động tốt hơn ở độ pH trung tính của nước thải.
Nhược điểm của phương pháp này chính là khối lượng bùn và muối kim loại trong bùn tăng lên.
Quá trình sẽ loại bỏ hoàn toàn Photpho ra khỏi nước thải nhờ phương pháp lắng.
Dùng phèn nhôm xử lý photpho theo phương trình hóa học như sau:
Al3+ + PO43+ ↔ AlPO4
Al3+ + 3OH– ↔ Al(OH)3
Sử dụng vôi:
5Ca2+ + 3PO43- + OH– ↔ Ca5(PO4)3(OH)
Mg2+ + 2OH– ↔ Mg(OH)2
Ca2+ + CO32- ↔ CaCO3
Sử dụng phèn sắt:
Fe3+ + PO43- ↔ FePO4
Fe3+ + 3OH– ↔ Fe(OH)3
Phương pháp sinh học
Quá trình xử lý photpho bằng phương pháp sinh học có thể đạt được bằng cách hoàn lưu bùn hoạt tính trong điều kiện kỵ khí và hiếu khí. Quá trình này giúp hình thành một quần thể vi sinh vật có khả năng lưu trữ Phốt pho nội bào dưới dạng Polyphosphat, gọi là các vi sinh vật PAO (polyphosphate-accumulating organisms). Nếu các vi sinh vật PAO này tồn tại với số lượng đủ lớn thì Phốt pho sẽ được loại bỏ cùng với bùn hoạt tính thải.
Quá trình EBPR
Trong thực tế khi xử lý photpho bằng phương pháp sinh học áp dụng quy trình kỵ khí khi tiếp nối với quy trình hiếu khí. Còn gọi là phương pháp loại bỏ photpho tăng cường EBPR (Enhanced biological phosphorus removal)
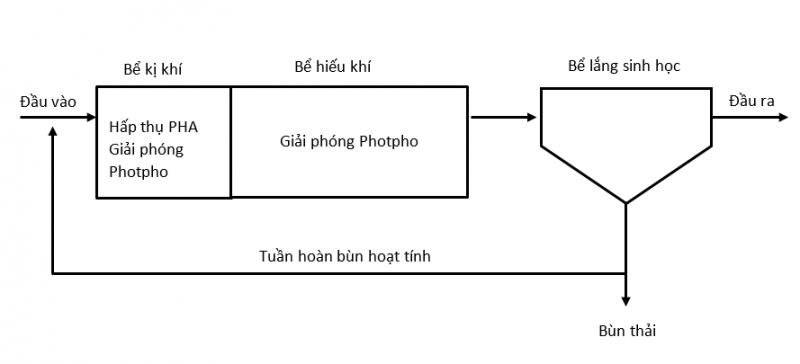
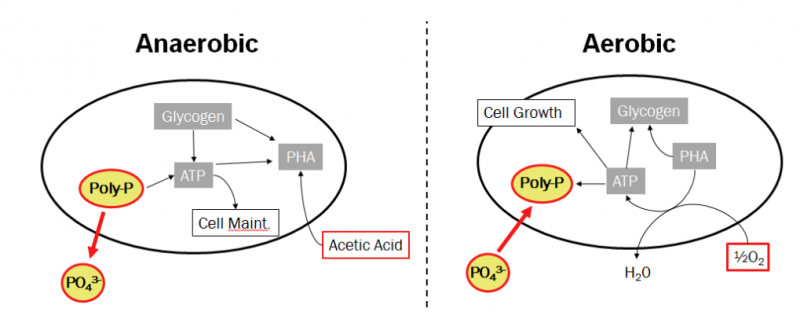
- Dưới điều kiện kị khí, PAOS không phát triển mà chuyển đổi các vật liệu hữu cơ đơn giản như axit béo dễ bay hơi (VFAs), chủ yếu được tạo ra bằng cách lên men vi sinh vật, thành các polyme giàu năng lượng được gọi là polyhydroxyalkanoate (PHA) phổ biến nhất các loại polyhydroxybutyrate (PHB) và polyhydroxyvalerate (PHV). Đồng thời giải phóng 1 lượng orthophotphat dự trữ bên trong tế bào.
- Trong điều kiện hiếu khí, vi khuẩn PAOs oxi hóa PHA và nguồn cacbon trong nước thải như nguồn năng lượng để phát triển tăng sinh khối, nhu cầu tổng hợp poly-P dự trữ tăng đồng thời tạo ra glycogen. Lượng poly-P tích lũy trong sinh khối có tỷ lệ cao đến 15% trọng lượng khô. Điều đáng chú ý là lượng photphat hòa tan được hấp thụ trong giai đoạn hiếu khí nhiều hơn là Photphat được giải phóng trong giai đoạn kỵ khí, dẫn đến giảm nồng độ P trong nước thải. P được loại bỏ cùng với lượng bùn thải sau khi lắng sinh học.
Các tế bào vi sinh tích lũy lượng dư P trong sinh khối tạo thành bông cặn lắng xuống đáy bể lắng, photpho chứa trong cặn được tháo ra ngoài đưa đi xử lý riêng, hoặc được dùng lại như là chất lên men để tác dụng với các axit béo bay hơi làm tăng hiệu quả quá trình khử photpho.
Quá trình Phostrip
Quá trình PhoStrip kết hợp quá trình sinh học và hóa học cho việc khử photpho. Phần lớn photpho trong bùn họat tính tuần hoàn được chuyển đến bể tách khí kị khí nơi mà photpho được giải phóng ở dạng hòa tan. Trong quá trình PhoStrip, hiệu quả khử photpho ít phụ thuộc vào nồng độ rbCOD đầu vào so với những quá trình khử photpho bằng phương pháp sinh học khác.
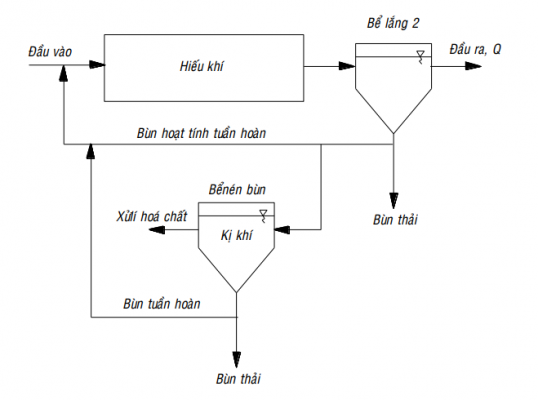
Hình mô tả PhoStrip
Kết hợp xử lý AMONI và Photpho bằng quá trình sinh học
Công nghệ A2/O
Công nghệ A2/O là viết tắt của cụm từ Anerobic (kỵ khí) – Anoxic (thiếu khí) – Oxic (hiếu khí). Công nghệ này là sự cải tiến của quá trính A/O. Kết hợp 3 hệ vi sinh: kỵ khí, thiếu khí, hiếu khí liên tục để tăng hiệu quả xử lý amoni và photpho. Một số loại vi sinh PAOs có khả năng sử dụng oxi trong Nitrat để hấp thụ P và phát triển sinh khối vì thế ở bể thiếu khí ngoài xử lý N cũng giảm được một lượng P đáng kể.
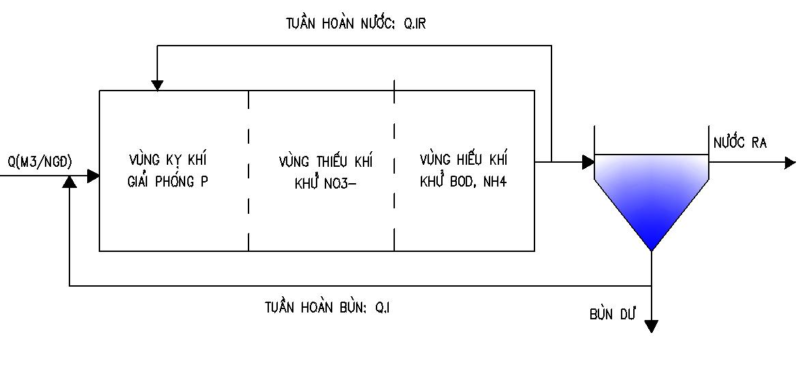
Hình mô tả mô hình A2O
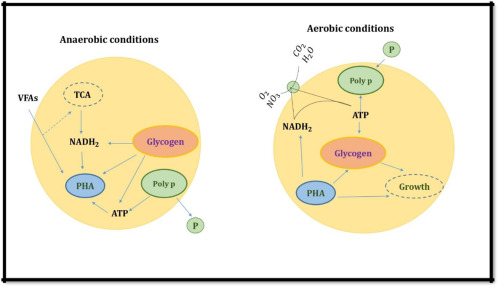
Hình mô tả vsv PAO tích lũy P ở anaerobic và anoxic
Quá trình UCT
Quá trình UCT được sáng tạo bởi trường đại học University of Cape Town. Quá trình UCT được phát triển để giảm đến mức tối thiểu sự ảnh hưởng của nitrat trong nước thải không đạt tiêu chuẩn vào vùng tiếp xúc kị khí. Lượng Nitrat trong vùng kị khí là quyết định hiệu quả khử photpho sinh học.
Quá trình UCT đối với quá trình A2/O có 2 sự khác biệt. Bùn hoạt tính được tuần hòan đến bậc thiếu khí thay vì bậc hiếu khí, và dòng nội tuần hòan từ bậc thiếu khí đến bậc kị khí. Bằng việc tuần hoàn bùn hoạt tính đến bậc thiếu khí, sự đưa nitrat đến bậc kị khí được lọai trừ, do đó sự hấp thu photpho trong bậc kị khí được tốt hơn. Đặc trưng của dòng nội tuần hoàn là làm tăng sự sử dụng chất hữu cơ trong bậc kị khí. Hỗn dịch từ bậc thiếu khí chứa nhiều BOD hòa tan nhưng nitrat ít. Tuần hoàn của hỗn dịch thiếu khí cung cấp điều kiện tối ưu cho sự lên men trong bậc kị khí.

Hình mô tả mô hình UCT
Quy trình Bardenpho (5 giai đoạn)
Từ bể Bardenpho 4 giai đoạn để xử lý Nitơ, bổ sung thêm 1 giai đoạn để kết hợp khử cả nitơ và photpho. Thêm giai đoạn thứ 5 là quá trình yếm khí anarobic để khử photpho lên đầu tiên của quy trình kết hợp khử nitơ, photpho. Sự sắp xếp các giai đoạn và cách tuần hoàn hỗn hợp nước thải sau các vùng cũng khác nhau và khác quy trình xử lý A2/O.
Hệ thống 5 bước cung cấp các vùng anaerobic, anoxic, aerobic để khử cả Nitơ, Photpho và hợp chất hữu cơ. Vùng Anoxic (giai đoạn 2) để khử nitrat và được bổ sung nitrat từ bể aerobic (giai đoạn 3). Bể aerobic cuối cùng tách khí N2 ra khỏi nước và giảm hàm lượng Photpho xuống tối đa. Thời gian xử lý kéo dài hơn quy trình A2/O. Tổng thời gian lưu nước là 10-40ngày, tăng sinh khối của vi sinh vật

Hình mô tả Bardenpho 5gđ
Kết hợp xử lý Amoni và Photpho bằng phương pháp kết tủa Struvite
Phương pháp kết tủa Struvite là phương pháp thu hồi Amoni và Photpho trong nước thải dưới dạng kết tủa tinh thể gồm 3 thành phần hóa học magiê, amoniac và phốt pho, còn được gọi tắt là MAP.
Công thức hóa học của struvite là Mg2+ + NH4+ PO4-3 + 6H2O -> NH4MgPO4.6H2O.
Hiệu suất thu hồi Struvite dựa vào tỷ lệ bão hòa MAP. Magiê, amoniac và phốt pho kết hợp trong nước theo tỷ lệ mol 1:1:1. Tuy nhiên, một trong các tỷ lệ trên thay đổi, pH dung dịch thay đổi thì hiệu suất và thành phần của kết tủa cũng thay đổi theo, và tinh thể struvite thu được cũng thay đổi theo công thức phân tử sau MgNH4PO4⋅nH2O (n = 1, 3, 6, 7).
Hầu hết các nguồn nước thải chứa rất ít ion Mg2+, để thu được kết tủa struvite, cần bổ sung ion Mg2+. Để đạt được các tỷ lệ phù hợp, các hóa chất có thể sẽ phải được bổ sung vào hệ phản ứng ví dụ: Na2HPO4.12H2O, MgCl2.6H2O và NaOH.
Các loại nước thải công nghiệp phù hợp để thu hồi struvite như: nước rỉ rác, nước thải chăn nuôi (phân gia súc, gia cầm), nước thải sinh hoạt, nước thải nhà máy sản xuất phân bón…

Hình mô tả struvite thu hồi trong nước thải
Các nghiên cứu gần đây cho thấy công nghệ kết tủa magie-amonia-photphat từ nước thải nhằm thu hồi amoni, phot pho không những hiệu quả về chi phí mà còn có ý nghĩa lớn về môi trường.
Struvite được biết đến là một dạng phân bón chậm tan cung cấp đồng thời nguyên tố đa lượng (N: 6% và P2O5: 28,9%) và nguyên tố trung lượng (Mg: 10%) phù hợp cho nhiều loại cây trồng nên struvite được sử dụng làm nguyên liệu để sản xuất các loại phân bón hỗn hợp hoặc phức hợp khác.
Như vậy, việc kết tủa struvite và các dẫn xuất của nó từ nước thải có chứa amoni, phốt pho được xem là phương pháp xử lý thân thiện với môi trường, loại bỏ đồng thời cả N và P từ nước thải và thu được sản phẩm có giá trị để phục vụ cho sản xuất nông nghiệp.
MPTEK chuyên cung cấp các giải pháp xử lý Amoni và Photpho trong nước thải công nghiệp, nước thải sinh hoạt, nước thải đô thị… Liên hệ với chúng tôi ngay để được tư vấn và tìm giải pháp tốt nhất cho bạn!
CÔNG TY TNHH GIẢI PHÁP MPTEK
Hotline: 0903188563
Địa chỉ: 20 Huỳnh Thiện Lộc, Phường Hòa Thạnh, Quận Tân Phú, TPHCM.